

Article paru dans le magazine Semper – édition Jan 2022 – www.dsb.lu
L’homme et la nature ne font qu’un et sont en perpétuelle évolution, à la recherche d’un équilibre qui implique un pouvoir d’adaptation hors du commun à tout ce qui se passe sur notre belle planète et qui se résume en un mot: la biodiversité. Et celle-ci a ses raisons d’être. Alors comment comprendre ces variants SARS-CoV-2 dont tout le monde parle ?
En résumé et en guise de rappel, nous voyons 3 acteurs sur scène:
1. Les virus (leur composition: une unité chimique). Ils peuvent être à ARN (Composé de Groupement phosphate, sucre, Uracile, Adénine, Guanine et Cytosine) ou à ADN (Composé de groupement phosphate, sucre désoxyribose, Thymine, Adénine, Guanine, Cytosine).
Pour se répliquer, les virus ont besoin d’un hôte, qui sont les deux autres acteurs:
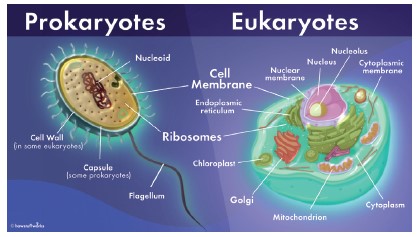
2. Les Procaryotes (organismes uni-cellulaires, bactéries, levures…).
3. Les Eucaryotes (organismes multicellulaires, caractérisés par une interrelation entre les différents types de cellules et un potentiel de génie génétique bien organisé: humains, animaux, plantes, végétations…).
Le scénario des infections cellulaires humaines peut être décrit en 6 étapes:
1. Au hit-parade des protéines (pour le moment), la protéine «Spike» (Protéine S) qui s’accroche au récepteur d’une cellule (ACE2), permettant ainsi de pénétrer dans les cellules ciblées.
2. Le virus se déshabille et libère (dans le cas du SARS-CoV-2) son ARN.
3. L’ARN est ensuite transformé en protéine par l’intermédiaire du génie génétique de la cellule hôte.
4. Réplication de la protéine afin de produire plus d’ARN.
5. Les protéines et l’ARN se recombinent pour former de nouveaux virions dans l’appareil de Golgi.
6. Un nouveau virus est libéré de la cellule hôte.
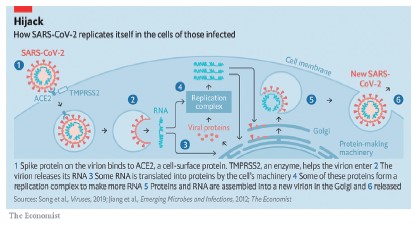
Ce type de réplication déroule des milliers de fois, et lors de ces cycles, des erreurs de réplication peuvent intervenir à différents endroits dans la structure de l’ARN. S’agit-il seulement d’erreurs? La question peut se poser. Et si, outre des erreurs accidentelles lors des réplications, il y avait également une intervention des défenses naturelles des cellules hôtes, intervenant dans la phase de réplication et affaiblissant ainsi l’action du virus d’origine ?
Notre système immunitaire a une très longue histoire d’adaptation au cours des siècles et il n’est pas près de nous laisser tomber, pour autant qu’on le respecte par notre manière de vivre.
La variabilité et la fréquence de l’apparition de variants observés dépend de multiples facteurs intrinsèques (génétiques, pharmacologiques - absorption/distribution/métabolisme/ excrétion, pharmacogénétiques, pharmacogénomiques, stress…) et extrinsèques (climat, culture, éducation, philosophies, migrations de populations, habitudes médicales, pollution, diététique…) propres à l’être humain, expliquant les variabilités entre populations, mais aussi les variations et mutations dans la nature et leurs influences chez l’homme. Cela explique également les variations de réactions diverses chez les personnes vaccinées suivant les populations.
Les avancées technologiques et le progrès des connaissances en pharmacogénétique chez l’humain nous permettront à moyen et long terme de disposer de traitements médicamenteux et de vaccins personnalisés, tenant compte des interactions médicamenteuses et des incompatibilités entre traitements. C’est la magistrale de l’avenir.
| «Notre système immunitaire a une très longue histoire d’adaptation au cours des siècles et il n’est pas près de nous laisser tomber, pour autant qu’on le respecte par notre manière de vivre.» |
Pour l’heure, afin de pouvoir rapidement évaluer la relation entre le génotype et les caractéristiques phénotypiques des différents variants, dans le but de mettre à jour les diagnostics, les vaccins et les thérapeutiques, il est indispensable d’organiser une surveil-lance épidémiologique moléculaire en temps réel. C’est la contribution de la plateforme GISAID (Global Initiative on Sharing Avian Influenza Data)1 qui depuis 2019 à séquencé plus de 450.000 génomes de variants SARS-CoV-2 et - surtout - partage ses données. L’union fait la force. Jacques BERLO
Référence:
1 Global Initiative on Sharing Avian Influenza Data (GISAID) est un projet qui a vu le jour le 24 août 2006, lorsqu’un groupe de chercheurs de renommée mondiale annonça la création d’une coalition internationale qui favoriserait le partage des données sur la grippe aviaire. Cette initiative fut annoncée dans une lettre publiée par la revue Nature, signée par plus de 70 scientifiques dont sept prix Nobel (ndlr, source wikipedia).

for articles/videos/studies
The articles can be sorted by therapeutic area or disease, but may also deal with more general topics not specifically related to a disease. These articles can be sorted as "other".